Sécurité alimentaire
Expliqué par des experts : Les 5 meilleurs conseils pour la quantification que vous devez connaître
Bienvenue dans la première série "Expliqué par des experts" avec April Englishbey, chef de produit mondial chez MDx.
Entrons tout de suite dans le vif du sujet et découvrons ce qu'est la quantification.
"J'ai participé à la quantification et au lancement commercial de la première méthode de quantification (ou kit), SalQuant™, et j'ai suivi toute l'aventure. J'ai donc voulu partager quelques expériences et attributs en tant que client, ce que vous devriez chercher à demander à votre fournisseur au sujet de la quantification.
En tant que personne ayant une expérience pratique du développement de la quantification pour l'industrie, je voulais partager les éléments critiques que nous prenons en compte lorsque nous commençons le développement de tout type de quantification, ainsi que la façon dont cela fonctionne pour l'industrie afin d'atteindre finalement l'objectif de réduction du risque pour le consommateur."
Conseil n° 1
"Le premier conseil est la flexibilité des données. Avec les données que vous cherchez à capturer et à utiliser, réfléchissez à ce que vous voulez réellement savoir. Lorsque vous obtenez un résultat de 5,7 UFC par gramme, comment l'utiliser comme outil de prise de décision ? C'est une partie de la découverte consultative que nous menons avec les clients pour aller à la racine de la façon dont vous avez besoin d'utiliser les informations supplémentaires".
Connaître la réponse à ces questions vous aide à décider laquelle des deux catégories de quantification vous convient le mieux en fonction de la flexibilité et de l'objectif des données.
- La véritable quantification, comme SalQuant, utilise un point de temps d'incubation identifié associé à un logiciel pour déterminer le nombre de bactéries dans l'échantillon original.
- Les tests de limites identifient simplement un résultat positif à un moment précis, indiquant que le nombre de bactéries est supérieur au seuil fixé. Ce type de test est parfois appelé "semi-quantitatif", mais les tests de limites et de seuils sont un peu moins confus.
Il est très important de bien comprendre le type de données que vous recherchez et la manière dont vous prendriez une décision en utilisant ces données ! En fin de compte, la méthode que vous utilisez a-t-elle la flexibilité d'utiliser un seul échantillon ou protocole pour effectuer des tests de quantification ou de limites ?
Deuxième conseil
"Le deuxième outil est l'option de matrice dynamique.
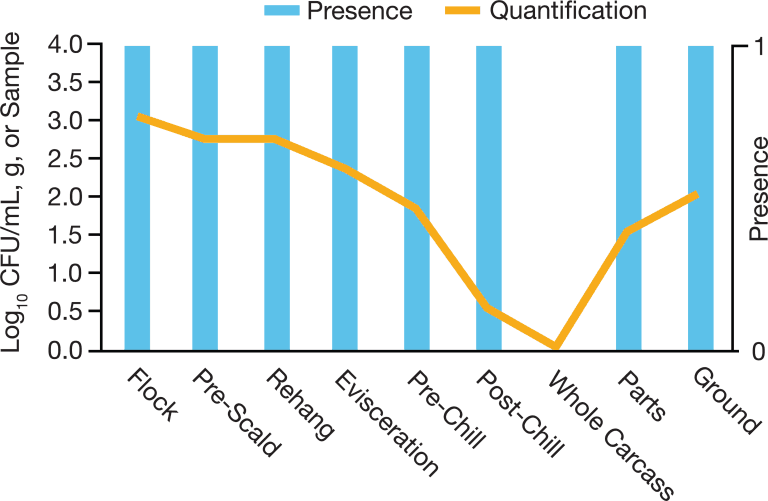
La sécurité alimentaire ne concerne pas uniquement les produits finaux, mais la plupart du temps, ce sont ces échantillons qui font l'objet de la plus grande attention. Cependant, la transformation et la pré-récolte font également partie de l'équation dont il faut se préoccuper pour gérer l'ensemble du domaine de la sécurité alimentaire.
Lorsque nous avons commencé ce voyage il y a trois ans, nous avons d'abord développé la quantification pour les produits finaux et recueilli des données intéressantes, MAIS nous devions encore comprendre pourquoi les bactéries survivaient encore après toutes les interventions appliquées tout au long du processus.
Si nous parvenons à assainir la production animale et alimentaire en amont, nous avons plus de chances d'éliminer les salmonelles tout au long du processus et de réduire ce risque. C'est la raison pour laquelle les industries et les personnes influentes ne se contentent pas de recueillir des données sur le produit final, mais ajoutent des points de données cohérents tout au long de leurs processus et évaluent réellement si les interventions sont efficaces. Nous avons également continué à travailler en amont, au niveau de la ferme ou avant la récolte, afin de mesurer l'impact que nous pouvons avoir sur la charge de Salmonella qui entre et qui sort.
Nous recherchons des fournisseurs dont les méthodes sont suffisamment robustes pour fonctionner dans diverses matrices et même dans le cas d'échantillons sales (par exemple, les produits de rinçage après réfrigération), les deux étant toujours des produits de rinçage, mais il faut vérifier que la méthode fonctionne en raison de la nature de la "saleté".
Tous les échantillons ne sont pas égaux, même s'ils se ressemblent. Il est donc important de s'assurer que des vérifications ont été effectuées pour voir les données par vous-même.
Troisième conseil
"Le troisième conseil concerne l'élargissement de l'éventail des possibilités de dénombrement.
Les méthodes doivent être capables d'atteindre l'extrémité inférieure (1 UFC) comme l'extrémité supérieure (10 000 UFC) de la plage de quantification, car nous avons besoin de flexibilité en fonction du type d'échantillon ainsi qu'en cas de défaillance critique due à une prolifération incontrôlée des bactéries".
Dans le cadre des programmes de sécurité alimentaire, nous savons qu'il y aura parfois une valeur aberrante (faible ou élevée) et que la méthode doit être capable de la quantifier plutôt que d'indiquer une valeur négative ou une valeur supérieure à la valeur dénombrable, ce qui n'est pas un point de données utile.
"J'aime utiliser l'exemple du rinçage, comme je l'ai mentionné dans le conseil n° 2, pour le contrôle du processus, afin de passer du sale au propre. Il est important de pouvoir quantifier le nombre élevé de bactéries avant l'intervention et le nombre très faible de bactéries après l'intervention, en sachant qu'elles sont toujours détectables et quantifiables, afin de mesurer réellement l'efficacité du processus et des interventions.
Il est vraiment important de comprendre que l'on attend d'un produit final qu'il soit le plus propre possible et le plus souvent exempt de pathogènes. Les résultats ne doivent pas se situer à des niveaux élevés comme 100 UFC/g ou mL. Même 10 UFC/g peuvent être trop élevés en fonction de l'industrie. Les méthodes dont la limite inférieure ne permet de quantifier que 100 UFC/g ne sont pas vraiment utiles pour un produit final, car l'utilisateur aura une fausse impression de "propreté" lorsque la quantification sera considérée comme négative.
Quatrième conseil
"Le quatrième conseil est que le processus doit être facile à utiliser.
D'un point de vue réglementaire, la prévalence sera toujours un élément essentiel pour mesurer le risque pour le consommateur, mais la quantification n'est pas censée remplacer totalement la prévalence. Il s'agit plutôt d'une valeur ajoutée. Lorsqu'il s'agit de répondre à des besoins réglementaires tout en recueillant davantage d'informations, l'utilisation d'un même échantillon tout au long du processus est très utile en termes de temps et de main-d'œuvre.
"L'utilisation d'un seul échantillon est essentiellement la raison pour laquelle nous avons conçu nos protocoles chez Hygiena pour avoir un flux de travail rationalisé où l'échantillon peut être configuré une fois pour obtenir les deux résultats de quantification, qui me disent si mon échantillon est positif avec un risque élevé, ou bien s'il est négatif et doit continuer à prévaloir pour gérer le risque réglementaire. La valeur de la quantification n'est pas censée perturber les processus normaux. Si vous ajoutez des ressources et des coûts supplémentaires ou de la main-d'œuvre, est-ce vraiment une valeur ajoutée en fin de compte ? Les données sont toujours très précieuses, mais si elles sont si difficiles à collecter en raison du processus, elles deviennent prohibitives. Nous avons besoin de données dynamiques, c'est-à-dire de données numériques, plutôt que d'avoir simplement des uns et des zéros ou des positifs et des négatifs.
Si ce n'est pas aussi facile à faire en laboratoire, les industries et les entreprises pourraient se contenter de faire le minimum de prévalence, ce qui n'est pas la voie à suivre en matière de sécurité alimentaire.
Cinquième conseil
"Le dernier conseil est de voir les données.
Pour toute méthode, il est important de prouver le succès avec des données provenant de validations ou de vérifications afin de s'assurer que les vendeurs et les développeurs de méthodes ont fait preuve de la diligence nécessaire.
"L'intérêt d'utiliser la PCR pour la quantification est que les tests ont déjà été validés pour l'élément central de la détection du pathogène à un niveau de 1 UFC/échantillon pour la prévalence, ce qui est plus difficile que la quantification. Comme toutes les cases ont déjà été cochées pour l'inclusivité et l'exclusivité, tout ce que nous faisons, c'est ajouter la quantification en utilisant des outils déjà établis pour la microbiologie".
Vous devez non seulement voir les données, mais aussi comprendre la quantité de données et la manière dont elles ont été collectées et comparées. Il ne suffit pas de développer ou de valider à partir de 10 échantillons, il faut au moins 30 échantillons pour créer une pertinence statistique et une confiance dans les comparaisons avec les méthodes de référence, mais il s'agit là d'un minimum absolu.
Récapitulons
La façon dont nous envisageons la quantification et les raisons qui sous-tendent tous ces types de questions et de commentaires que vous pouvez entendre dans l'industrie et au sein du gouvernement est de vous assurer que vous disposez de vos propres informations et de votre propre sensibilisation.
"L'utilisation d'un seul échantillon est essentiellement la raison pour laquelle nous avons conçu nos protocoles chez Hygiena afin d'avoir un flux de travail rationalisé où l'échantillon peut être configuré une fois pour obtenir les deux résultats de quantification, qui me disent si mon échantillon est positif avec un risque élevé, ou bien s'il est négatif et doit continuer à prévaloir pour gérer le risque réglementaire. La valeur de la quantification n'est pas censée perturber les processus normaux. Si vous ajoutez des ressources et des coûts supplémentaires ou de la main-d'œuvre, est-ce vraiment une valeur ajoutée en fin de compte ? Les données sont toujours très précieuses, mais si elles sont si difficiles à collecter en raison du processus, elles deviennent prohibitives. Nous avons besoin de données dynamiques, c'est-à-dire de données numériques, plutôt que d'avoir simplement des uns et des zéros ou des positifs et des négatifs.
Si ce n'est pas aussi facile à faire en laboratoire, les industries et les entreprises pourraient se contenter de faire le minimum de prévalence, ce qui n'est pas la voie à suivre en matière de sécurité alimentaire.